近年大數據與演算法讓著床前胚胎基因檢測(PGT)快速進化:從已知致病、單基因突變等聚焦於「確定性的遺傳異常」,到近年發展出將多基因風險導入胚胎挑選的應用。技術前沿的推進,卻也帶來新的問題:科學證據夠不夠?臨床幫助有多大?如何兼顧倫理與公平?接下來,讓我們一起了解 PGT 的演進,以及目前「能做什麼、還不能做什麼」。
從 PGD 到 PGT-A/M/SR,再到 PGT-P:胚胎基因檢測 30 年的進化史
表一統整了 PGT 的演進:早期多以 PGD 泛稱植入前的「特定風險」檢測(多見於家族已知致病突變/單基因疾病);後來逐步細分為 PGT-A(非整倍體)/PGT-M(單基因)/PGT-SR(結構重排);而近年的 PGT-P 則嘗試以多基因疾病的「相對風險(PRS)」做胚胎挑選的排序。

什麼是PGT-P?
PGT-P(Preimplantation Genetic Testing for Polygenic Risk)是透過計算多基因風險分數(polygenic risk score,PRS)來評估胚胎對多基因疾病(如糖尿病、冠狀動脈心臟病、乳癌、精神疾病等)的相對罹病風險,並依據此風險進行排序,優先選擇風險較低的胚胎進行植入的一項檢測。
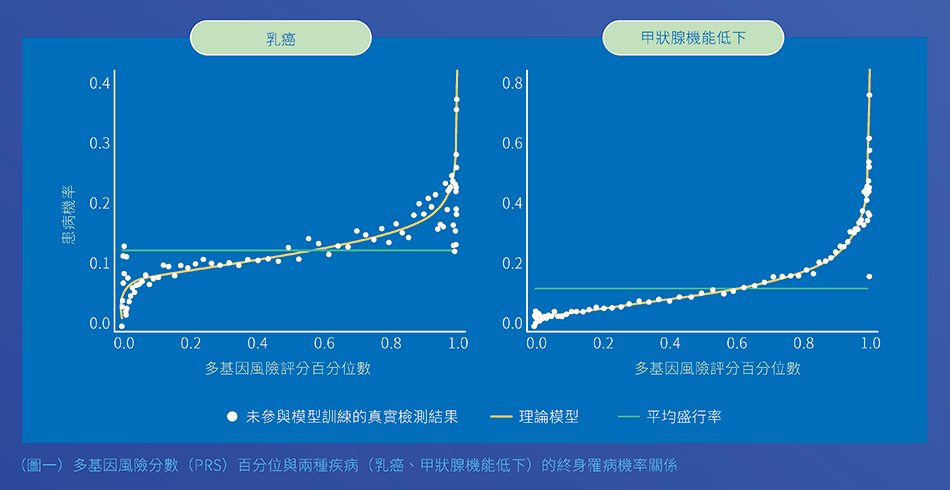
2021 年發表在《Genes》期刊上的一項研究1,顯示PRS 越高者,發病機率確實較高;反之,PRS 低者風險顯著下降。用乳癌、甲狀腺機能低下兩種疾病做範例,強調 PRS 可區分族群內高低風險個體(圖一)。
需要強調的是:
- PGT-P 與既有的 PGT-A/M/SR(非整倍體、單基因、結構重排)性質不同:後者多屬高風險、可明確診斷的遺傳異常。
- 複雜疾病受多基因與環境共同影響;PRS 只涵蓋部分遺傳成分,族群差異與環境仍會影響準確度。
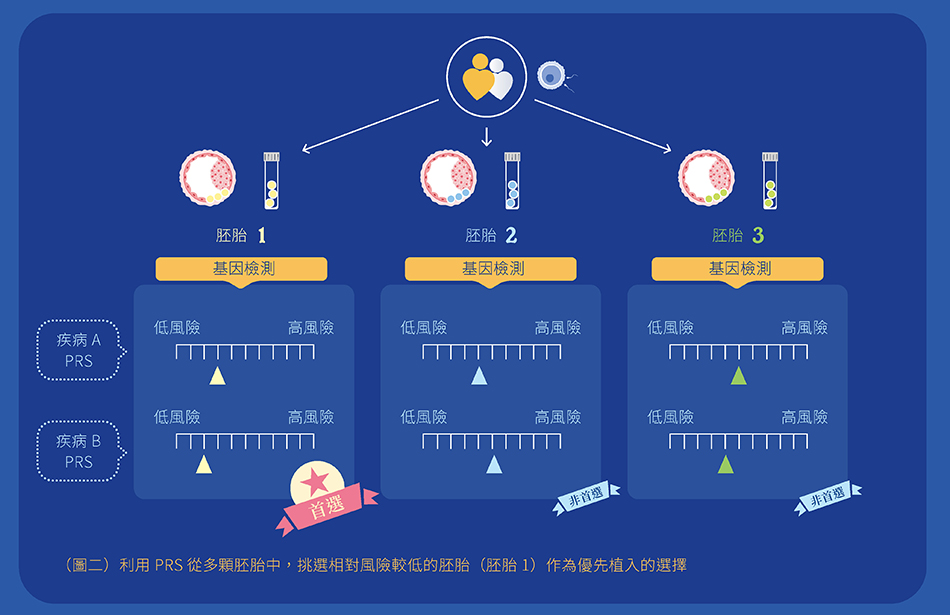
- PGT-P 估計的是機率的相對風險,不是「有或無」的診斷2(圖二)。

想像未來應用的場景
- 「一站式」的胚胎體檢:
- 進行PGT 檢測時,將不再只是排除「明確突變異常」的胚胎,而是獲得一份整合了罕見單基因變異、染色體異常以及成千上萬個微小基因變異位點(SNP)的綜合報告。這意味著一次檢測就能評估從遺傳病到常見慢性病(心臟病、糖尿病)的所有風險。
- 從「預防疾病」走向「特徵挑選」:
- 身高預測:告訴父母,胚胎 A 長大後預計會比胚胎 B 高出 5 公分以上(準確率約 80%)
- 智力與外貌:雖然目前主要在倫理討論階段,但未來可能會面臨父母要求篩選「認知能力」或「美容特徵」的情況,將引發社會與倫理辯論
- 社會階層的健康差距與普及化:
- 初期:檢測最初只有富人可負擔,導致其後代不僅享有更好的教育,還擁有更健康的基因(更少疾病、更長壽命),加劇社會不平等
- 後期:檢測逐漸普及,被納入國家健康保險或標準醫療程序,減少罹患慢性病(如糖尿病、高血壓)機率、降低國家的醫療支出
回到現實
PGT-P 回應了科學家「大幅降低遺傳疾病風險」的期待,但現階段因費用(每顆胚胎大約 2,500 ~ 5,000 美元不等)與準確性、倫理等等問題;距離「明確改善臨床結局」仍有漫漫長路要走。但我們始終相信科學與倫理可以找到平衡點——以審慎、實證、透明為原則,讓科技真正為家庭帶來福祉。
參考資料:
1. Tellier, L. C. A. M., Eccles, J., Treff, N. R., Lello, L., Fishel, S., & Hsu, S. (2021). Embryo screening for polygenic disease risk: Recent advances and ethical considerations. Genes, 12(8), 1105.
2. Capalbo, A., de Wert, G., Mertes, H., Klausner, L., Coonen, E., Spinella, F., Van de Velde, H., Viville, S., Sermon, K., Vermeulen, N., Lencz, T., & Carmi, S. (2024). Screening embryos for polygenic disease risk: A review of epidemiological, clinical, and ethical considerations. Human Reproduction Update, 30(5), 529–557. https://doi.org/10.1093/humupd/dmae012